Snatrium, met elementensymbool Sc en atoomnummer 21, is gemakkelijk oplosbaar in water, kan reageren met heet water en verkleurt gemakkelijk in de lucht. De hoofdvalentie is +3. Het wordt vaak gemengd met gadolinium, erbium en andere elementen, met een lage opbrengst en een gehalte van ongeveer 0,0005% in de aardkorst. Scandium wordt vaak gebruikt voor de productie van speciaal glas en lichtgewicht hogetemperatuurlegeringen.
Momenteel bedragen de bewezen scandiumreserves in de wereld slechts 2 miljoen ton, waarvan 90~95% zich bevindt in bauxiet-, fosforiet- en ijzertitaniumertsen, en een klein deel in uranium-, thorium-, wolfraam- en zeldzame aardmetalenertsen, voornamelijk gedistribueerd in Rusland, China, Tadzjikistan, Madagaskar, Noorwegen en andere landen. China is zeer rijk aan scandiumbronnen, met enorme minerale reserves gerelateerd aan scandium. Volgens onvolledige statistieken bedragen de scandiumreserves in China ongeveer 600.000 ton, die zich bevinden in bauxiet- en fosforietafzettingen, porfier- en kwartsaderwolfraamafzettingen in Zuid-China, zeldzame aardmetalenafzettingen in Zuid-China, Bayan Obo zeldzame-aardijzerertsafzetting in Binnen-Mongolië en Panzhihua vanadiumtitaniummagnetietafzetting in Sichuan.
Door de schaarste aan scandium is de prijs ervan ook erg hoog. Op het hoogtepunt was de prijs zelfs tien keer zo hoog als die van goud. Hoewel de prijs van scandium is gedaald, is deze nog steeds vier keer zo hoog als die van goud!
Geschiedenis ontdekken
In 1869 merkte Mendelejev een verschil in atomaire massa op tussen calcium (40) en titanium (48), en voorspelde dat er zich hier ook een onontdekt element met een intermediaire atomaire massa bevond. Hij voorspelde dat het oxide ervan X₂O₅ is. Scandium werd in 1879 ontdekt door Lars Frederik Nilson van de Universiteit van Uppsala in Zweden. Hij won het uit de zwarte zeldzame goudmijn, een complex erts dat 8 soorten metaaloxiden bevat. Hij heeftErbium(III)oxideuit zwart zeldzaam gouderts, en verkregenYtterbium(III)oxidevan dit oxide, en er is een ander oxide van een lichter element, waarvan het spectrum aangeeft dat het een onbekend metaal is. Dit is het metaal voorspeld door Mendelejev, waarvan het oxide isSc₂O₃Het scandiummetaal zelf werd geproduceerd uitScandiumchloridedoor elektrolytisch smelten in 1937.
Mendelejev
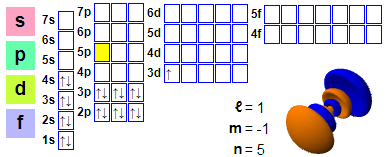
Elektronenconfiguratie
Elektronenconfiguratie: 1s2 2s2 2p6 3s2 3p6 4s2 3d1
Scandium is een zacht, zilverwit overgangsmetaal met een smeltpunt van 1541 ℃ en een kookpunt van 2831 ℃.
Gedurende een aanzienlijke periode na de ontdekking ervan werd het gebruik van scandium niet aangetoond vanwege de productiemoeilijkheden. Met de toenemende verbetering van methoden voor de scheiding van zeldzame aardmetalen is er nu een volwassen processtroom voor de zuivering van scandiumverbindingen. Omdat scandium minder alkalisch is dan yttrium en lanthanide, is hydroxide het zwakst. Het gemengde mineraal met zeldzame aardmetalen dat scandium bevat, wordt daarom van het zeldzame aardmetalen gescheiden door middel van de "stapprecipitatie"-methode, waarbij scandium(III)hydroxide na overbrenging in oplossing met ammoniak wordt behandeld. De andere methode is het scheiden van scandiumnitraat door middel van polaire ontleding van nitraat. Omdat scandiumnitraat het gemakkelijkst te ontleden is, kan scandium worden gescheiden. Daarnaast is de uitgebreide winning van het bijbehorende scandium uit uranium, thorium, wolfraam, tin en andere minerale afzettingen ook een belangrijke bron van scandium.
Nadat een zuivere scandiumverbinding is verkregen, wordt deze omgezet in ScCl Å en gesmolten met KCl en LiCl. Het gesmolten zink dient als kathode voor elektrolyse, waardoor scandium neerslaat op de zinkelektrode. Vervolgens wordt het zink verdampt om metallisch scandium te verkrijgen. Dit is een lichtgewicht zilverwit metaal met zeer actieve chemische eigenschappen, dat kan reageren met heet water om waterstofgas te genereren. Het metaalscandium dat u op de foto ziet, is daarom in een fles verpakt en beschermd met argongas, anders vormt scandium snel een donkergele of grijze oxidelaag, waardoor het zijn glanzende metaalglans verliest.
Toepassingen
Verlichtingsindustrie
De toepassingen van scandium zijn geconcentreerd in zeer heldere richtingen, en het is geen overdrijving om het de Zoon van het Licht te noemen. Het eerste magische wapen van scandium is de scandium-natriumlamp, die kan worden gebruikt om duizenden huishoudens licht te brengen. Dit is een metaalhalide elektrische lamp: de lamp is gevuld met natriumjodide en scandiumtrijodide, en scandium en natriumfolie worden tegelijkertijd toegevoegd. Tijdens hoogspanningsontlading zenden scandiumionen en natriumionen respectievelijk licht uit met hun karakteristieke emissiegolflengten. De spectraallijnen van natrium zijn 589,0 en 589,6 nm, twee beroemde gele lichten, terwijl de spectraallijnen van scandium 361,3~424,7 nm zijn, een reeks van emissies van nabij-ultraviolet en blauw licht. Omdat ze elkaar aanvullen, is de algehele geproduceerde lichtkleur wit licht. Juist omdat scandiumnatriumlampen de eigenschappen van een hoge lichtopbrengst, een mooie lichtkleur, energiebesparing, lange levensduur en een sterk mistremmend vermogen hebben, zijn ze breed inzetbaar voor televisiecamera's, pleinen, sportterreinen en straatverlichting. Ze staan bekend als lichtbronnen van de derde generatie. In China wordt dit type lamp geleidelijk aan gepromoot als een nieuwe technologie, terwijl het in sommige ontwikkelde landen al begin jaren 80 op grote schaal werd gebruikt.
Het tweede magische wapen van scandium zijn fotovoltaïsche zonnecellen, die het op de grond verstrooide licht kunnen opvangen en omzetten in elektriciteit om de menselijke samenleving te stimuleren. Scandium is het beste barrièremetaal in metaalisolator-halfgeleider-silicium zonnecellen en zonnecellen.
Het derde magische wapen is de γ A-stralingsbron. Dit magische wapen kan op zichzelf fel schijnen, maar dit soort licht kan niet met het blote oog worden waargenomen; het is een hoogenergetische fotonenstroom. We extraheren 45Sc meestal uit mineralen, de enige natuurlijke isotopen van scandium. Elke 45Sc-kern bevat 21 protonen en 24 neutronen. 46Sc, een kunstmatige radioactieve isotoop, kan worden gebruikt als γ-stralingsbron of traceratomen, en kan ook worden gebruikt voor radiotherapie van kwaadaardige tumoren. Er zijn ook toepassingen zoals de yttrium-gallium-scandium-granaatlaser.ScandiumfluorideGlasvezel, infrarood, optische vezel en scandium-gecoate kathodestraalbuis op televisie. Het lijkt erop dat scandium geboren wordt met helderheid.
Legeringsindustrie
Scandium in zijn elementaire vorm wordt veel gebruikt voor het doperen van aluminiumlegeringen. Zolang er maar een paar duizendsten scandium aan aluminium worden toegevoegd, ontstaat er een nieuwe Al3Sc-fase, die een rol speelt in de metamorfose van aluminiumlegeringen en de structuur en eigenschappen van de legering aanzienlijk verandert. Het toevoegen van 0,2% tot 0,4% Sc (wat vergelijkbaar is met de hoeveelheid zout die thuis aan roergebakken groenten wordt toegevoegd; er is maar een klein beetje nodig) kan de rekristallisatietemperatuur van de legering met 150-200 °C verhogen en de sterkte bij hoge temperaturen, de structurele stabiliteit, de lasprestaties en de corrosiebestendigheid aanzienlijk verbeteren. Het kan ook het fenomeen van verbrossing voorkomen dat gemakkelijk kan optreden bij langdurig gebruik bij hoge temperaturen. Aluminiumlegeringen met een hoge sterkte en hoge taaiheid, nieuwe corrosiebestendige lasbare aluminiumlegeringen met een hoge sterkte, nieuwe aluminiumlegeringen met hoge temperaturen, aluminiumlegeringen met een hoge sterkte die bestand zijn tegen neutronenbestraling, enz. hebben zeer aantrekkelijke ontwikkelingsperspectieven in de lucht- en ruimtevaart, luchtvaart, schepen, kernreactoren, lichte voertuigen en hogesnelheidstreinen.
Scandium is ook een uitstekende modificator voor ijzer, en een kleine hoeveelheid scandium kan de sterkte en hardheid van gietijzer aanzienlijk verbeteren. Daarnaast kan scandium ook worden gebruikt als additief voor hoogtemperatuur wolfraam- en chroomlegeringen. Naast het maken van bruidskleding voor anderen, heeft scandium een hoog smeltpunt en is de dichtheid vergelijkbaar met die van aluminium. Het wordt ook gebruikt in lichtgewicht legeringen met een hoog smeltpunt, zoals scandium-titaniumlegering en scandium-magnesiumlegering. Vanwege de hoge prijs wordt het echter over het algemeen alleen gebruikt in hoogwaardige productie-industrieën, zoals spaceshuttles en raketten.
Keramisch materiaal
Scandium, een enkelvoudige stof, wordt over het algemeen gebruikt in legeringen, en de oxiden ervan spelen op een vergelijkbare manier een belangrijke rol in keramische materialen. Tetragonaal zirkoniumoxide, een keramisch materiaal dat kan worden gebruikt als elektrodemateriaal voor vaste-oxide brandstofcellen, heeft de unieke eigenschap dat de geleidbaarheid van deze elektrolyt toeneemt met toenemende temperatuur en zuurstofconcentratie in de omgeving. De kristalstructuur van dit keramische materiaal zelf kan echter niet stabiel zijn en heeft geen industriële waarde; het is noodzakelijk om stoffen te doteren die deze structuur kunnen fixeren om de oorspronkelijke eigenschappen te behouden. Het toevoegen van 6-10% scandiumoxide lijkt op een betonstructuur, waardoor zirkoniumoxide kan worden gestabiliseerd op een vierkant rooster.
Er zijn ook keramische materialen zoals siliciumnitride, dat zeer sterk en hittebestendig is, als verdichtingsmiddelen en stabilisatoren gebruikt.
Als verdichter,ScandiumoxideKan een refractaire Sc2Si2O7-fase vormen aan de rand van fijne deeltjes, waardoor de vervorming van technische keramiek bij hoge temperaturen wordt verminderd. Vergeleken met andere oxiden kan het de mechanische eigenschappen van siliciumnitride bij hoge temperaturen beter verbeteren.
Katalytische chemie
In de chemische technologie wordt scandium vaak gebruikt als katalysator, terwijl Sc2O3 kan worden gebruikt voor dehydratie en deoxidatie van ethanol of isopropanol, de ontleding van azijnzuur en de productie van etheen uit CO en H2. De Pt-Al-katalysator met Sc2O3 is ook een belangrijke katalysator voor de zuivering en raffinage van zware olie in de petrochemische industrie. Bij katalytische kraakreacties zoals met cumeen is de activiteit van de Sc-Y-zeolietkatalysator 1000 keer hoger dan die van de aluminiumsilicaatkatalysator. Vergeleken met sommige traditionele katalysatoren zijn de ontwikkelingsvooruitzichten voor scandiumkatalysatoren zeer gunstig.
Kernenergie-industrie
Door een kleine hoeveelheid Sc2O3 toe te voegen aan UO2 in de kernbrandstof van een hogetemperatuurreactor, kunnen roostertransformatie, volumetoename en scheurvorming als gevolg van de omzetting van UO2 in U3O8 worden voorkomen.
Brandstofcel
Op vergelijkbare wijze zal het toevoegen van 2,5% tot 25% scandium aan nikkel-alkalibatterijen de levensduur ervan verlengen.
Landbouwveredeling
In de landbouw kunnen zaden zoals maïs, bieten, erwten, tarwe en zonnebloemen worden behandeld met scandiumsulfaat (de concentratie is over het algemeen 10-3~10-8 mol/l; verschillende planten hebben verschillende resultaten). Het daadwerkelijke effect van het bevorderen van de kieming is bereikt. Na 8 uur nam het droge gewicht van de wortels en knoppen met respectievelijk 37% en 78% toe ten opzichte van zaailingen, maar het mechanisme wordt nog onderzocht.
Van Nielsens aandacht voor de waarde van atomaire massadata tot vandaag de dag, is scandium pas honderd of twintig jaar in het gezichtsveld van mensen gekomen, maar het heeft bijna honderd jaar op de bank gelegen. Pas met de krachtige ontwikkeling van de materiaalkunde aan het einde van de vorige eeuw bracht het hem tot leven. Tegenwoordig zijn zeldzame aardmetalen, waaronder scandium, grote sterren geworden in de materiaalkunde. Ze spelen een steeds veranderende rol in duizenden systemen, brengen ons dagelijks leven meer gemak en creëren een economische waarde die nog moeilijker te meten is.
Plaatsingstijd: 29 juni 2023